Killer
Allgemeine Schockformen:
- Blutung, Volumenverlust (Hypovolämer Schock)
- Sepsis, Anaphylaxie (Distributiver Schock)
- Myokardinfarkt, tachykarde / bradykarde Rhythmusstörung, Herzinsuffizienz (Kardiogener Schock)
- Spannungspneumothorax, Lungenembolie, Perikardtamponade (Obstruktiver Schock)
Besondere Schockformen (kausale Einteilung, primär symptomatische Therapie): z.B. Toxischer Schock, Endokriner Schock und Neurogener Schock
Red Flags
- Schweißigkeit, Blässe
- Subjektive Atemnot ("Lufthunger"), Tachypnoe
- Puls nicht/schwach tastbar
- Marmorierung/Rekap-Zeit ≥ 4 sek.
- Neu aufgetretene Agitation/Delir/Desorientiertheit
- Hypotonie
- Tachykardie oder Bradykardie
(initiale Tachykardie wird plötzlich bradykard: CAVE: Peri-arrest-Situation!) - Niedriger / abfallendes etCO2
Erste Schritte
- Kreislaufstabilisierung - auch wenn Ursache initial unklar ist:
- Fokussierte Untersuchung + Anamnese (cABCDE, Fokus auf C):
- Klinisch Hyper- oder Hypovolämie?
- Rhythmusstörung? (Breitkomplextachykardie? Relevante Bradykardie?)
- V.a. Sepsis? (Fieber/Infektzeichen?)
- Notfall-Sonografie (z.B. RUSH-Protokoll)
- BGA und breites Labor (inkl. Laktat, Hb, CRP/PCT, Troponin, TSH)
- 12-Kanal-EKG (Ischämiezeichen: STEMI, Hochrisiko-EKG/OMI? Rhythmusstörung?)
- Fokussierte Therapie nach vermuteter Genese/Schockform
Hypovolämer Schock
- Blutstillung bei kritischer Blutung nach innen oder außen (Interventionen, Endoskopie oder OP brauchen Vorbereitungszeit!)
- Frühzeitig (Massiv)transfusion und Gerinnungstherapie einleiten
- Massiver Volumenmangel (Exsikkose, Erbrechen/Diarrhö): 10-20ml/kg VEL iv.
Distributiver Schock
- V.a. Sepsis: Blutkulturen + Antibiose schnellstmöglich
- VEL 10-20ml/kg iv.
- dann nach Klinik frühzeitig Noradrenalin-Perfusor
- Anaphylaxie: sofort Adrenalin 0,5mg im.
Kardiogener Schock
- Myokardinfarkt: ASS 250mg iv. + Heparin 70IE/kg iv., rasch Herzkatheter
- Rhythmusstörung:
- Bei Bradykardie frühzeitig (externes) Pacing, überbrückend Adrenalin 10-20µg iv. siehe PushDose Pressor
- Bei Tachykardie frühzeitig elektrische Kardioversion
Obstruktiver Schock
- LAE: Lysetherapie
- Pneumothorax: Entlastungspunktion, Thoraxdrainage
- Perikardtamponade: Entlastungspunktion, ggf. Thorakotomie
Tipps
- Klinisches Bild zählt! Hypotonie, Tachykardie, Tachypnoe, Marmorierung unklarer Ursache → V.a. Schock!
- Marmorierung zeigt sich oft zunächst an den Knien (= Decke hoch!)
- Schock bedeutet nicht immer Hypotonie - und Hypotonie nicht automatisch Schock
“Kryptogener Schock” = noch normaler Blutdruck bei peripherer Minderperfusion (z.B. kardiale Schockformen, Bradykardie + Ersatzrhythmus, Kinder) - Initial Stabilisierung und Diagnostik parallel, fokussiertes Vorgehen nach cABCDE
- Kritische Blutung sofort stillen (Tourniquet, Druckverband, etc.)
- Lebensrettende Tools: RUSH-Sono, PushDose Pressors, BGA
- CAVE: Die übliche nichtinvasive automatische Blutdruckmessung (oszillometrische Messung) überschätzt oft den Blutdruck bei Hypotonie (falsch hohe Messung)!
Frühzeitig invasive arterielle Blutdruckmessung erwägen, auch präklinisch (falls verfügbar).
- Neue / unklare Hypotonie (auch ohne objektivierbare Schockzeichen) sollte abgeklärt und kritisch evaluiert werden!
Fokus Präklinik
- Red Flags prüfen, Killer aktiv erwägen
- Erste Schritte, insb.:
- Zugang, Volumen, ggf. Pushdose Pressor
- Fokussierte (cABCD-) Untersuchung inkl. EKG
- Spezifische Therapie fokussiert - Schocktherapie nach möglicher Ursache:
- Hypovolämie: Blutung stillen, Volumengabe, ggf. TXA
- Kardiogen: Rhythmusstörung ggf. elektrisch kardiovertieren, frühzeitig 12-Kanal EKG: STEMI/OMI?
- Sepsis: Volumen, Noradrenalin-Perfusor, rascher Transport
- Obstruktiv:
- H.a. Pneumothorax - Thoraxdrainage
- Hochgrad. V.a. Lungenembolie - Lyse erwägen
- Transportziel: Klinik mit kompetenter Intensivmedizin / nichttraumatologischem Schockraum
- Voranmeldung!
Schock - Flowchart
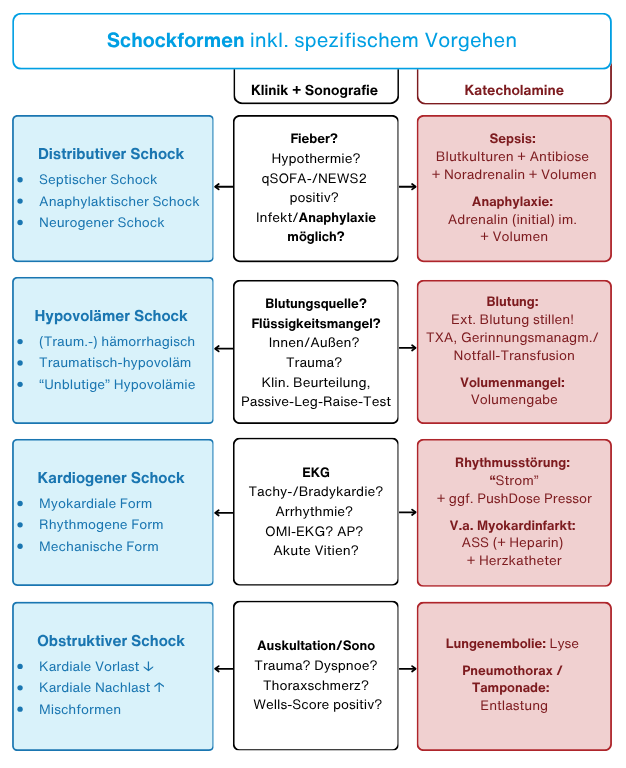
→ Detail-Flowchart: GuruFacts Schock
Monitoring
Parameter zur Therapiesteuerung:
- Klinik: Besserung von Vigilanz/Rekap.-Zeit relevant und häufig zugunsten von physikalischen Messwerten übersehen
- etCO2: Erniedrigtes etCO2 bei reduziertem Herzzeitvolumen und/oder Lungenembolie
- Auch außerhalb der Lungenembolie gut als ein Baustein zur Verlaufsbeurteilung in der Initialphase nutzbar
- Laktat: im Schock unspezifischer Marker von Gewebe-Minderperfusion.
Anstieg ev. auch bei Intoxikation mit erhöhter Anionenlücke oder bei Adrenalin-Gabe- CAVE: hohes Laktat nicht pauschal mit Volumendefizit gleichsetzen
- Verlaufskontrollen zur Therapiekontrolle, Ziel: Laktat↓
- MAP (mittlerer arterieller Druck): Ziel >65mmHg
- Immer in Kontext mit Klinik/Vorerkrankungen betrachten (Bsp: Chronischer Hypertonus braucht meist auch im Schock höheren MAP)
- Diurese
- Stundendiurese ist zwar guter Verlaufsparameter, in der Notaufnahme jedoch zu träge und daher eher zur langfristigen Verlaufsbeobachtung geeignet.
Volumenstatus und -gabe
Bei V.a. Volumenmangel: 20ml/kg iv. VEL innerhalb der ersten Stunde unter engmaschiger Verlaufskontrolle.
Bei Hämorrhagie: Frühzeitig Transfusion + Gerinnungstherapie (statt Verdünnung durch Volumengabe)
- Volumenmangel wird insb. bei Sepsis oft überschätzt
- Steuern der Volumentherapie möglichst über dynamische Verlaufsparameter
- Initiale Beurteilung der Volumenreagibilität behelfsmäßig über Blutdruck möglich
Eigentliche Fragestellung: Gibt es noch eine Volumentoleranz? Volumenüberlastung bei fehlender Volumentoleranz erhöht die Mortalität!
Volumenbeurteilung
Klinische Beurteilung (z.B. Ödeme oder trockene Schleimhäute) können in der Einschätzung helfen, sind aber in der Initialphase oft allein nicht ausreichend. Wichtig ist v.a. die Volumenreagibilität und Volumentoleranz.
Dynamische Parameter
Passive-Leg-Raise-Test:
- Beine bei flach liegender Patient:in um 45° für 90 Sekunden anheben
- Anstieg des MAP/RRsyst um >10mmHg hinweisend für Volumenreagibilität
Falls Herzfrequenz rückläufig und Blutdruck ansteigend bzw. Arterienkurve in Variabilität vermindert / etCO2 leicht ansteigend: Patient:in könnte von erneutem Volumenbolus profitieren
Änderung des Schlagvolumens/HZV:
- Echokardiografische Messung möglich - Messung vor nach Volumengabe zur Verlaufsbeurteilung notwendig bzw. VTI-Messung vor und nach Passive Leg Raise
Beurteilung der V. cava inferior:
- Bei ausgeprägten Befunden (atemstarre, pralle VCI oder komplett kollaptische VCI) potentiell aussagekräftig
- Insb. „intermediäre Befunde“ oder bei bekannter Rechtsherzinsuffizienz / hochgradiger Trikuspidalklappeninsuffizienz / Beatmung mit hohem PEEP allerdings kaum zur alleinigen Beurteilung nutzbar
- Ggf. als Verlaufsbeurteilung in Zusammenschau mit Klinik, Blutdruckverlauf sowie Laktat geeignet
Nicht allein zur Steuerung der Volumentherapie in der Notfallsituation empfohlen:
- ZVD
- Zentralvenöse Sättigung
Erweiterte Möglichkeiten zur Bestimmung des Volumenstatus sind u.a. komplexere sonografische Techniken (z.B. VExUS) oder Meßmethoden, die meist v.a. in der Intensivmedizin (z.B. Pulskonturanalyse) verfügbar sind.
Katecholamine
Die Gabe von Katecholaminen ist oft zentral in der Therapie des Schocks.
Primäres Katecholamin in der Notaufnahme: Noradrenalin (zur Überbrückung ggf. als PushDose Pressor, dann im Verlauf via Perfusor)
Inotropika: Dobutamin, alternativ ggf. Levosimendan
Therapierefraktärer Schock trotz Katecholamin-Gabe - Ursachen
verschiedene Gründe möglich, z.B.:
- "Technisches" Problem
- venöser Zugang liegt paravasal
- Problem mit Perfusor / -leitung
- Medizinisches Problem
- Azidose
- Anaphylaxie
- Persistierende Blutung
- Intoxikation (z.B. Betablocker, Trizyklika)
- Hypokalzämie
Schockformen
Überblick und pathophysiologische Konzepte bei Schock (vereinfacht nach Standl et. al 2018)
Schockform | Pathophysiologie | |
|---|---|---|
Hypovolämer Schock Häufigkeit | Subformen:
| ad 1: Blutung mit (relevantem) Verlust von Erythrozyten ad 2: (Poly-) Trauma, etc.: ad 3: Flüssigkeitsverlust / verminderte Flüssigkeitszufuhr ad 4: Flüssigkeitsverlust |
Distributiver Schock Häufigkeit | Subformen:
| Relative Hypovolämie durch ad 1: Periphere Vasodilatation, Volumenverschiebung, ad 2: Akute Vasodilatation ad 3: (Massive) Vasodilatation |
Kardiogener Schock Häufigkeit | Subformen:
| Reduktion der effektiven kardialen (Pump)leistung ad 1: Reduzierte Pumpfunktion ad 2: Tachykarde Rhythmusstörungen ad 3: Herzklappenerkrankungen |
Obstruktiver Schock Häufigkeit | Subformen:
| Obstruktion großer Gefäße bzw. Herz ad 1: Diastolische Füllungsbehinderung ad 2: Obstruktion der aortalen Strombahn ad 3: Obstruktion Pulmonalgefäße |
Mischformen | Verschiedene Schockformen sind erschwert einer klassischen Schockform zuzuordnen, z.B.: | |
Kardiogener Schock
Komplexes Krankheitsbild, in der Früherkennung auch oft übersehen, hohe Letalität insb. bei verzögerter Diagnostik und Therapie: Frühzeitige Rücksprache und Zusammenarbeit mit Kardiologie und Intensivmedizin!
Klinische Formen des kardiogenen Schocks (vereinfacht):
- "Klassiker": verminderte Pumpleistung, Hypotonie, Tachykardie
→ Typisch: Akuter Myokardinfarkt plus Hypotonie und/oder Perfusionsdefizit (z.B. Oligurie, verlängerte Rekap.-Zeit, hohes Laktat, Wesensveränderung) - „Spezialfall“: Normotensiver/kryptogener Schock (ca. 25% der Patient:innen): Periphere Vasokonstriktion bei reduziertem Herzzeitvolumen - deutlich erhöhte Nachlast belastet den linken Ventrikel zusätzlich. Schock mit Minderperfusion kann trotz MAP > 65mmHg / RRsyst > 90mmHg vorliegen!
Ursachen des kardiogenen Schock
- Kardiogen
- Okklusiver Myokardinfarkt (z.B. STEMI)
- Postinfarktkomplikationen (hochgradige Mitralklappeninsuffizienz bei Papillarmuskelabriss, Ventrikelseptumruptur)
- Herzrhythmusstörung (Brady- und Tachykardien)
- (Akute) Vitien (hochgradige Mitralklappeninsuffizienz, hochgradige Aortenklappenstenose etc.)
- Perikardtamponade
- "Nicht kardiogen" (de facto eigene Schockformen)
- Septische Kardiomyopathie (wichtig: Überschneidungen möglich bzw. gemeinsame Endstrecke: Patient:innen mit kardiogenem Schock können ein ausgeprägtes SIRS mit Multiorganversagen, Pat. mit Sepsis können eine septische Kardiomyopathie entwickeln)
- Intoxikation mit Betablockern / Trizyklischen Antidepressiva / Calciumantagonisten
- Lungenembolie
- Pneumothorax
Checkliste Kardiogener Schock
- Kontakt Kardiologie / Intensivmedizin → gemeinsame Absprache bei Therapie
(falls keine Kardiologie verfügbar: Kontaktaufnahme nächstes Zentrum)
- Diagnostik / Monitoring:
- EKG (Tachykardie? Bradykardie? Ischämiezeichen?)
- Labor (inkl. BGA/Laktat, Troponin, BNP, Nieren- und Leberwerte)
- Arterielle Blutdruckmessung
- Echokardiografie:
- Orientierend / "Basis-Echo": Linksventrikuläre Pumpfunktion? Rechtsherzbelastung? Perikardtamponade? Infarktkomplikationen: neue Vitien? Ventrikelruptur?
- Bei Erfahrung: Bestimmung Cardiac Index (CI) / Cardiac Power Index (CP), peripherer Widerstand (SVRI)
- Therapie - Stabilisierung (Ziel ist kausale Therapie!)
- Volumenchallenge erwägen (z.B. 200ml VEL iv.), zuvor ggf. Passive Leg Raise und/oder engmaschige Überwachung von Monitoring, vorher/nachher Echo (s. Volumentherapie oben)
- Katecholamine (Ziel MAP 65-75mmHg, rückläufiges Laktat)
s. Perfusoren- Vasopressor: Noradrenalin
insb. bei peripherer Gefäßdilatation / hyperdynamen LV - Inotropikum: Dobutamin (alternativ z.B. Levosimendan)
insb. bei eingeschränkter LV-EF
- Vasopressor: Noradrenalin
- Frühzeitig invasive Beatmung erwägen
- Narkose-Einleitung = Hochrisiko-Situation (physiologisch schwieriger Atemweg), Bedingungen vorab optimieren!
- Überbrückend ggf. NIV-Beatmung
- Therapie - Kausal
- Primäres Ziel: Ursachenbehebung z.B. Revaskularisierung durch Herzkatheter, Therapie der Rhythmusstörung oder operative Revaskularisierung / Behandlung des Vitiums
- Möglich keine / geringestmögliche Zeit-Verzögerung - ohne kausale Therapie ist kein positives Outcome zu erwarten!
Weiterführende Literatur und Links
Interessante Links (frei zugänglich)
- Ethische Aspekte im Rahmen von extrakorporalen Herz-Kreislauf- Unterstützungssystemen (ECLS) (DGK, DGTHG, DGAI 2024)
- VExUS Sonografie Übersichtsartikel (Ultrasound Journal 2024)
- Infografik Schock (Nerdfallmedizin 2022)
- Leitlinie Extrakorporale Zirkulation ECLS/ECMO (AWMF 2020)
- Leitlinie Infarktbedingter Kardiogener Schock (AWMF 2019)
- Schockformen und Tipps aus der Praxis (Nerdfallmedizin 2018)
- Understanding lactate in sepsis (EMcrit 2015)
Literatur
- Dutzmann, J. et al. Ethische Aspekte im Rahmen von extrakorporalen Herz-Kreislauf-Unterstützungssystemen (ECLS): Konsensuspapier der DGK, DGTHG und DGAI. Die Kardiologie 18, 353–364 (2024).
- Assavapokee, T., Rola, P., Assavapokee, N. & Koratala, A. Decoding VExUS: a practical guide for excelling in point-of-care ultrasound assessment of venous congestion. Ultrasound J. 16, 48 (2024).
- Riessen, R., Bulla, P., Mengel, A. & Kumle, B. Initiale Diagnostik und Therapie des Schocks. Med. Klin. - Intensiv. Notfallmedizin 1–9 (2024).
- Perera, Y., Raitt, J., Poole, K., Metcalfe, D. & Lewinsohn, A. Non-invasive versus arterial pressure monitoring in the pre-hospital critical care environment: a paired comparison of concurrently recorded measurements. Scand. J. Trauma, Resusc. Emerg. Med. 32, 77 (2024).
- DGTHG. S3-Leitlinie Extrakorporale Zirkulation (ECLS / ECMO), Einsatz bei Herz-und Kreislaufversagen. AWMF. (2020).
- Fandler, M. & Gotthardt, P. Schock: Differenzialdiagnostik und Therapie in der Präklinik. Kardiologie up2date 16, 197–199 (2020).
- DGK. S3-Leitlinie Infarktbedingter kardiogener Schock - Diagnose, Monitoring Therapie. AWMF (2019).
- Standl, T. et al. The Nomenclature, Definition and Distinction of Types of Shock. Dtsch. Ärzteblatt Int. 115, 757–768 (2018).
- Janssens, U. et al. Empfehlungen zum hämodynamischen Monitoring in der internistischen Intensivmedizin. Kardiologe 10, 149–169 (2016).
- Seif, D., Perera, P., Mailhot, T., Riley, D. & Mandavia, D. Bedside Ultrasound in Resuscitation and the Rapid Ultrasound in Shock Protocol. Crit. Care Res. Pr. 2012, 503254 (2012).