Killer
- Akutes Koronarsyndrom (ACS)
- Aortensyndrom
- Lungenembolie
- Pneumothorax
- Ösophagusruptur
Red Flags
- Kaltschweißigkeit, Übelkeit
- Dyspnoe
- Vigilanzminderung
- Neurologische Ausfälle (auch intermittierend)
- Tachykardie
- Bradykardie
- Schock
- Wiedervorstellung mit rezidivierenden / erneuten Thoraxschmerzen
- Schmerzen trotz adäquater Analgesie / überproportionaler Schmerz
Erste Schritte
- Immer kontinuierliches Monitoring + frühzeitig EKG
- V.a. STEMI/OMI/Hochrisiko-EKG: Herzkatheter + Defibrillationsbereitschaft
- Erste Schritte bei STEMI/OMI: Merkhilfe "AHAB" s. unten
(ASS, Heparin, Analgesie, evtl. Betablocker)
- Erste Schritte bei STEMI/OMI: Merkhilfe "AHAB" s. unten
- Unspezifischer EKG-Befund + andauernde Beschwerden: nach 20min Verlaufs-EKG, nach Troponin-Verlauf (bei vielen hochsensitiven Assays mittlerweile „1h-Algorithmus“ möglich; jeweils individuelle Grenzwerte)
- V.a. STEMI/OMI/Hochrisiko-EKG: Herzkatheter + Defibrillationsbereitschaft
- O2-Gabe: Bei Hypoxie (SpO2 ≤90%), Dyspnoe oder Schock
- Fokussierte Untersuchung - Hinweis auf kritische Diagnose?
- ACS: Thoraxschmerz oder -druck, Ausstrahlung in linken/rechten Arm oder Hals/Kiefer, Übelkeit, Atemnot
- Aortensyndrom: Reißender/plötzlicher Schmerz, „Thoraxschmerz +1“
- Lungenembolie: Sinustachykardie, TVT, Rechtsherzbelastung (EKG/Echo)
- Kardiogener Schock: Vigilanzminderung/Unruhe, Kaltschweißigkeit, verlängerte Rekap.-Zeit/Marmorierung (kardiogener Schock auch bei Normotension möglich)
- Labor inkl. vBGA, Troponin
bei DD Lungenembolie: ggf. D-Dimere / Risikostratifizierung (PERC/YEARS)
- Bildgebung
- Fokussiertes Sono (Herz, Thorax, Aorta): Aus-/Einschluss kritischer DD
- Röntgen-/CT-Thorax nach klinischem Verdacht (CT sofort bei V.a. Aortensyndrom)
Differenzialdiagnostik bei Thoraxschmerz - Strukturiertes Vorgehen
- Lebensbedrohliche Ursache? ("Killer")
- ACS
- Aortensyndrom
- Ösophagusruptur
- Lungenembolie
- Pneumothorax
- Progress oder neue Komplikation chronischer kardiopulmonaler Erkrankung? z.B.
- Instabile Angina Pectoris bei KHK
- Pleuraerguss
- Symptomatische Anämie bei bestehender KHK
- Aortenklappenstenose
- Koronarspasmen
- Akute kardiopulmonale Erkrankung mit spezifischer Therapieindikation? z.B.
- Myokarditis, Perikarditis
- Tako-Tsubo-Kardiomyopathie (→Pschyrembel)
- Kardiales Trauma (Contusio cordis)
- Pneumonie, Pleuritis
- Schlaganfall
- Andere akute, nicht kardiopulmonale Erkrankung? z.B.
- Gastrointestinale Beschwerden (Gastroösophagealer Reflux, Ösophagusspasmen, peptisches Ulkus, heptobiliäre Erkrankung)
- Muskuloskelettale Beschwerden, Lumbago
- Herpes Zoster (thorakal)
- Psychogene Genese (u.a. Panikstörung) - Ausschlussdiagnose
Hinweise bei Untersuchung und Risikofaktoren
Hinweise auf Diagnosen bei fokussierter körperlicher Untersuchung:
- Kardiale Dekompensationszeichen: Abgeschwächtes Atemgeräusch (Pleuraerguss?), Beinödeme, feuchte Rasselgeräusche (Lungenödem?)
- Beinumfangsdifferenz (TVT → Lungenembolie?)
- Fokale neurologische Ausfälle (ggf. auch intermittierend) / pulsierende abdominelle Masse / reißende oder wandernde Schmerzen / massive Blutdruckdifferenz an den Armen (Aortendissektion?)
- Halsvenenstauung: (Lungenembolie? Spannungspneumothorax? Perikardtamponade?)
- Zeichen von Minderperfusion als Hinweis auf einen kardiogenen Schock (auch bei Normotension möglich): Vigilanzminderung/Bewusstseinsstörung, Kaltschweißigkeit, verlängerte Rekap.-Zeit, Unruhe
- Perikardreiben (Perikarditis?), leise Herztöne / Niedervoltage (Perikarderguss?)
"Typische" Risikofaktoren bei kritischen Diagnosen:
- ACS: >40J, bekannte KHK, Diabetes Mellitus, Arterielle Hypertonie, Hypercholesterinämie, Nikotin
- Aortensyndrom: Z.n. Aorten-OP / Herzkatheter, Marfan-Syndrom, Ehler-Danlos-Syndrom (o. Ä.)
- Lungenembolie: Z.n. LAE / TVT, Tumorerkrankung (aktiv), Z.n. OP / Immobilisation, orale Kontrazeptiva, Schwangerschaft
- Pneumothorax: <40J, Z.n. Pneumothorax, Nikotin
Tipps
- Selten „klassische“ Vorgeschichte oder typische Präsentation aus dem Lehrbuch. Auch bei Fehlen klassischer Risikofaktoren: Thoraxschmerz immer ernst nehmen!
- Nicht stur an Troponin-Grenzwerten "festhalten". Bei klinischem Verdacht und insb. bei persistierender Symptomatik: Weitere Überwachung / Diagnostik!
- Bei unklarem EKG / klinischem Verdacht auf ACS ohne Ischämie-Nachweis im „Routine-12-Kanal-EKG“: Erweiterte EKG-Ableitungen (V7-9, rechts)
- Neue Bezeichnung “OMI” (okklusiver Myokardinfarkt) inkludiert “klassischen” STEMI und ACS mit Hochrisiko-EKG (“STEMI-Äquivalente”) → beide gleiche Dringlichkeit!
- Keine Diagnose "erfinden": Ein offensichtlich muskuloskelettaler Thoraxschmerz darf natürlich als solcher benannt werden. Wenn die Ursache aber unklar ist, sollte das auch in der (Verdachts-)Diagnose so benannt werden (z.B. "Thoraxschmerz unklarer Genese"), sonst werden Pat. und ev. nachfolgende Kolleg:innen auf falsche Fährten gelockt.
Fokus Präklinik
- Red Flags prüfen, Killer aktiv erwägen
- Erste Schritte, insb.:
- Monitoring + 12-Kanal-EKG: STEMI oder Hochrisiko-EKG?
- Sauerstoff bei SpO2 <94% oder bei Schockzeichen
- STEMI/OMI oder instabil: Defi-Patches kleben!
- Spezifische Therapie fokussiert
- ACS
- STEMI / Hochrisiko-EKG ("OMI"): ASS 250mg iv., Heparin 5000IE iv.
- ACS ohne STEMI/Hochrisiko (kein OMI): evtl. ASS; primär kein Heparin!
- V.a. Aortensyndrom z.B. bei "Thoraxschmerz plus eins" - insb. wandernder Schmerz, Synkope(n), (intermittierende) neurologische Ausfälle
- Kein ASS / Heparin, RR und HF „normal“ halten, Analgesie
- ACS
- Transportziel:
- ACS: Klinik mit Kardiologie + 24h Herzkatheter, Voranmeldung!
- Verlaufs-EKG schreiben: Dynamik?
- V.a. Aortensyndrom: Klinik mit Herz-/Gefäßchirurgie, Voranmeldung!
- ACS: Klinik mit Kardiologie + 24h Herzkatheter, Voranmeldung!
Akutes Koronarsyndrom - ACS
- STEMI/OMI → Notfall-Herzkatheter ohne Troponin abzuwarten
- NSTE-ACS → Nach Flowchart (s. unten, hier 1h-Algorithmus mit hsTroponin) inkl. Troponin-Dynamik und Risikostratifizierung
Hintergrund OMI / STEMI
- Alleiniges Nicht-Erfüllen der STEMI-Kriterien ist nicht ausreichend für den Ausschluss einer akut interventionspflichtigen Koronarokklusion!
- Relevanter Anteil der NSTEMI-Patient:innen hat- wie bei „echtem“ STEMI - akute Koronarokklusionen und profitiert von frühzeitiger Intervention
- Klassifikation „OMI“ = Okklusiver Myokardinfarkt umfasst daher nicht nur klassischen STEMI, sondern auch eine Reihe weiterer Hochrisiko-EKGs, welche mit akut interventionspflichtigen Koronarokklusionen einhergehen
- Bei NOMI hingegen kann potenziell (je nach Risikostratifizierung, Klinik, Troponin-/EKG-Dynamik etc.) wie bei „klassischem“ NSTEMI auch im Verlauf evaluiert bzw. interveniert werden.
- Einteilung „OMI“ hat rein formal noch keinen Einzug in die Leitlinien erfahren, ein zunehmendes Umdenken findet jedoch auch außerhalb der Notaufnahmen und in der Kardiologie statt
- Jedoch: inzwischen höhere Wertigkeit von "Hochrisiko-NSTEMIs" in den neuesten ESC-ACS Guidelines und durch die Aufnahme einzelner Hochrisiko-EKGs als sogenannte „STEMI-Äquivalente“ in die Leitlinien
- Begriff „STEMI-Äquivalent“ wird ebenfalls kontrovers diskutiert, da er nach wie vor eine STEMI-zentrierte Denkweise impliziert, statt die jeweiligen Hochrisiko-EKGs auch begrifflich als eigene OMI-Entität darzustellen.
- Im Gespräch mit traditionelleren bzw. konservativen kardiologischen Kolleg:innen hat der Begriff „STEMI-Äquivalent“ oder "Hochrisiko-NSTEMI" aktuell vermutlich (noch) mehr Erfolg als der Begriff „OMI“
Alle STEMIs sind OMIs. Aber nicht alle OMIs sind STEMIs.
CAVE: Frauen haben häufig nicht den klassischen Lehrbüchern entsprechende Symptome bei ACS!
ACS bei Frauen - Symptomatik
- Im Vergleich zu männlichen Patienten stellen sich Frauen erst später nach Symptombeginn vor (im Durchschnitt 1h später)
→ Diagnose und Therapie ist bei Frauen oft verzögert! - Häufige keine klassischen „lehrbuchartigen“ linksthorakalen Schmerzen, sondern „Angina-Äquivalente“, u.a.
- Abdominelle Beschwerden (insb. Oberbauch)
- Brennender retrosternaler Schmerz (evtl. als Sodbrennen fehlinterpretiert/-diagnostiziert)
- Ausstrahlung in Hals / Kiefer
- Atemnot
- Übelkeit / Erbrechen
- Schwindelgefühl
Wichtig: Aufmerksam sein und nicht auf die „klassischen" Beschwerden fokussieren!
EKG
STEMI-Definition = ST-Hebungen in ≥2 benachbarten Ableitungen ≥1mm, außer:
- V2-V3 (etwas höhere ST-Hebungen tolerabel)
- ♂︎ <40 J.: ≥2,5mm
- ♂︎ ≥40 J.: ≥2mm
- ♀:︎ ≥1,5mm
- V7-V9: ≥0,5 mm
- V3r / V4r: ≥1 mm
Typische "zusammenhängende" Ableitungen
- I/aVL (lateral)
- II/III/aVF (inferior, auch als "Hinterwand" bezeichnet)
- V1/2 (anterior - Vorderwand, septal, evtl. rechtsventrikulär)
- V3/4 (antero-apikal)
- V5/6 (antero-lateral)
Sonderfälle (siehe auch "Hochrisiko-EKG"):
- aVL und V2 (hoch-lateral)
Hochrisiko-EKG / Hochrisiko-NSTEMI / "OMI"
Beispiele: s. "Hochrisiko-EKG"
- „SEMI-STEMI“ (noch nicht signifikante ST-Hebungen)
- Hyperakute T-Wellen
- De-Winter-Zeichen
- Wellens-Zeichen
- Shark-Fin-Zeichen
- (neuer) Linksschenkelblock (mod. Sgarbossa-Kriterien können hilfreich sein)
- (neu aufgetretener) Rechtsschenkelblock
- Hoher Lateralinfarkt (ST-Hebungen aVL und V2, evtl. auch ST-Hebung I und ST-Senkung III) auch "South African Flag Sign"
- Aslanger-Zeichen (isolierte ST-Hebung in III, ST-Senkung mindestens einer Ableitung V4-V6 mit positiv / terminal positiver T-Welle), ST-Strecke V1 > V2)
- „Hauptstamm-EKG“ (ST-Hebung in aVR, Senkungen in ≥6 Ableitungen - DD diffuse subendokardiale Ischämie bei Schock / Typ2-Myokardinfarkt)
STEMI-Mimics
„Mimics“ sind EKG-Bilder, die einen STEMI imitieren können, aber primär keine Herzkatheter-Untersuchung benötigen, sondern anderen Therapie oder Abklärung.
Primär gilt daher immer: Korrelation von EKG und Patient:in bzw. Symptomatik / Anamnese.
Kritische STEMI-Mimics
- Intrakranielle Blutung (evtl. ausgeprägte T-Negativierung)
- Aortendissektion (evtl. teils intermittierende ST-Hebungen, ggf. über mehrere Versorgungsgebiete)
- Hyperkaliämie (spitze T-Wellen bis hin zu QRS-Verbreiterung)
- Lungenembolie (Sinustachykardie, T-Negativierungen v.a. über der Vorderwand)
Dringliche STEMI-Mimics
- Hyperkalzämie
- Brugada-Syndrom
- ARVD/ARVCM
- Hypertroph-Obstruktive Kardiomyopathie (HOCM)
- Hypothermie
- Perimyokarditis
- Tako-Tsubo-Kardiomyopathie
- Intoxikationen (z.B. Trizyklika-Intox)
Andere / seltenere STEMI-Mimics
- Bestehendes Ventrikel-Aneurysma
- QRS-Verbreiterung bei Blockbildern
- Herzschrittmacher-EKG
- Frühe Repolarisation
- Myokardiale Tumorinfiltration
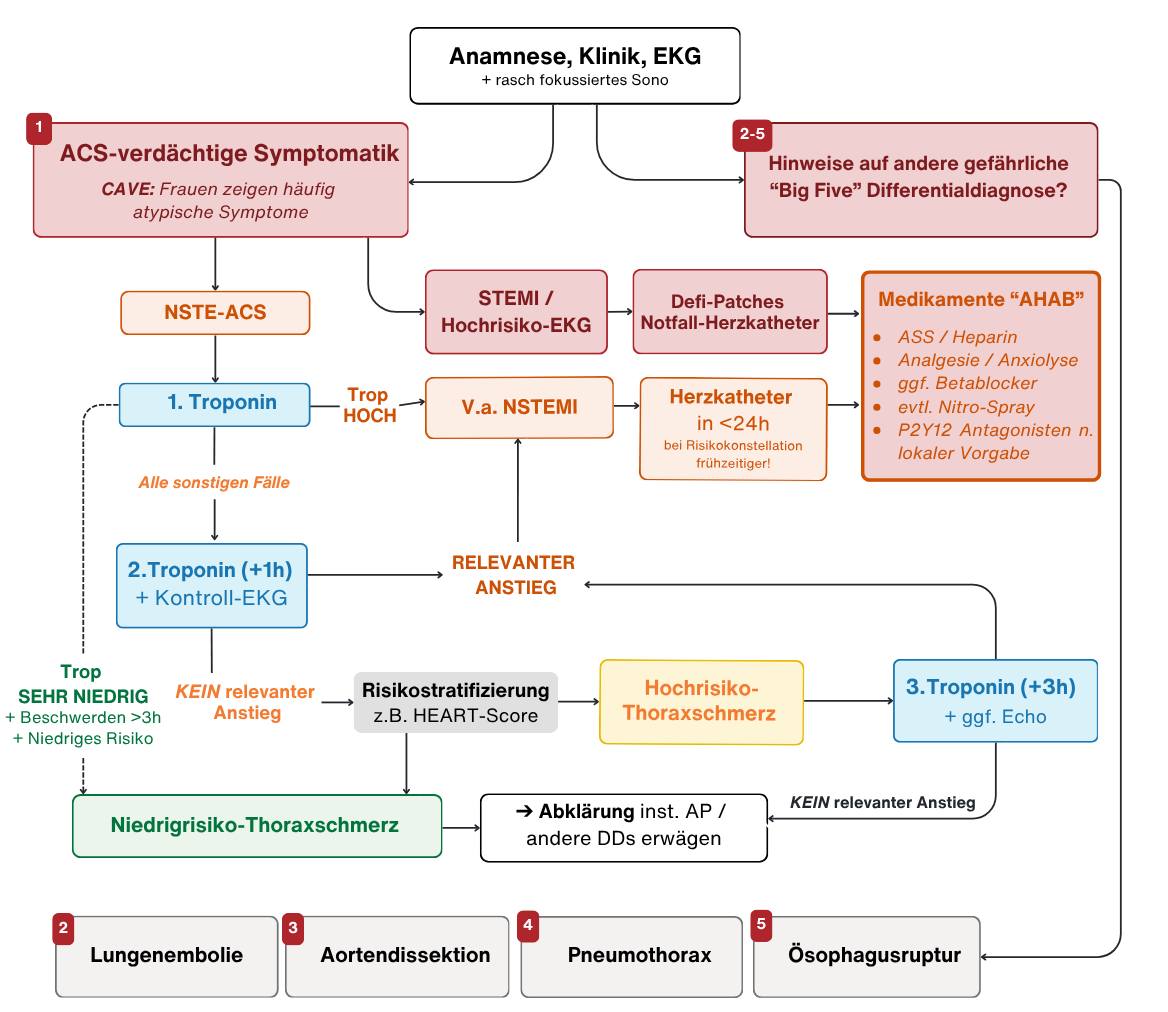
→ Detail-Flowchart: GuruFacts Thoraxschmerz - ACS
1h "Rapid Rule Out" Algorithmus - Hintergrund
Je nach im Labor verwendetem Troponin-Assay kann mittlerweile in vielen Kliniken das von der ESC empfohlene "1h-Algorithmus" verwendet werden (lokale Vorgaben / Empfehlungen beachten!). Hier immer Troponin = hochsensitives Troponin (hsTn).
Es gibt im Algorithmus vier relevante Troponin-Werte (jeweils unterschiedliche numerische Werte, nach verwendetem Assay):
- "very low" Wert (wenn Beschwerden >3h und "very low") Ausschluss NSTEMI (Evaluation Differenzialdiagnosen, Entlassung ggf. möglich ohne Verlaufskontrolle)
- "high" Wert: Hochgradiger V.a. NSTEMI, zeitnah Herzkatheter; bei Schock / persistierender Symptomatik notfallmäßig
- "Graubereich" (zwischen "very low" und "high") - hier Verlaufskontrolle 1h nach initialer Abnahme, dann weitere Entscheidung
- "Relevantes Delta" (relevanter Anstieg).
- Falls relevanter Anstieg: V.a. NSTEMI
- Falls kein relevanter Anstieg: Risikostratifizierung und Erwägung anderer Ursachen für erhöhtes Troponin?
- CAVE: Bei niedrigem (aber nicht "very low") initialem Wert kann es einen relevanten Anstieg geben und die beiden Werte trotzdem noch unterhalb der 99. Percentile (meist interner Labor-Grenzwert für "erhöhtes Troponin") liegen. Dann unbedingt klinische Kontrolle und trotzdem Risiko-Stratifizierung → Kein automatischer "Ausschluss"!
- "Relevantes Delta" (relevanter Anstieg).
Einige wichtige Punkte zum 1h-Algorithmus (via ESC ACS-Leitlinie):
- Kritische Diagnose: 1h-Algorithmus nur nutzen, wenn keine akut interventionspflichtige Pathologie vorliegt (z.B. STEMI oder OMI / Hochrisiko-EKG, akutes Aortensyndrom)
- Nur bei V.a. ACS: 1h-Algorithmus nur bei V.a. / DD ACS nutzen, nicht bei allen Notaufnahme-Patient:innen.
- Bei sehr früh vorstellenden Pat. (<2h nach Beginn der Beschwerden) könnte v.a. bei erhöhtem Risikoprofil eine Troponin-Kontrolle nach 3h (also 0-1-3h) sinnvoll sein.
- Bei negativen Troponinen und gleichzeitig hohem klinischen Verdacht (oder erneut auftretenden Beschwerden) erneute / serielle Troponinkontrolle erwägen.
- Die Stunden-Angaben beziehen sich auf den Zeitpunkt der Blutentnahme und nicht auf die Zeit, an dem die Blutprobe im Labor entgegebengenommen wurde. Es kann also sein, dass die zweite Troponinentnahme erfolgt, bevor der erste Wert abgeschlossen ist (insb. bei Blutentnahme durch den Rettungsdienst).
- Wichtig: Der Rapid-Rule-Out 1h (oder 2h-)Algorithmus gilt nur für validierte Assays (s. Tabelle in der ESC Leitlinie).
Risikostratifizierung
z.B. mit HEART-ScoreDiese Rechenhilfe findest du in der Notfallguru-App (s. Tabelle unten) oder →T-MACS-Score
HEART Score
HEART Score
HEART Score RechenhilfeDiese Rechenhilfe findest du in der Notfallguru-App
- <4 Punkte: Verlaufs-Troponin nach Schema, falls negativ: Entlassung möglich (bezüglich V.a. ACS, andere Differenzialdiagnosen müssen separat abgearbeitet/erwogen werden!)
- ≥4 Punkte: Erhöhtes Risiko: Stationäre Aufnahme, weitere Abklärung, Troponin-Verlauf
0 Pkt | 1 Punkt | 2 Punkte | |
|---|---|---|---|
History typisch für ischämischen Brustschmerz? | Atypisch | Mäßig typisch (atypische + typische Aspekte) | Typisch |
EKG ST-Veränderungen? | Normal | Unspezifisch veränderte Repolarisation z.B. bei LSB, LV-Hypertrophie | Signifikante ST-Hebungen oder ST-Senkungen ohne LSB, LV-Hypertrophie oder Digoxin |
Alter | < 45 Jahre | 45-65 Jahre | > 65 Jahre |
Risikofaktoren
| 0 Faktoren | 1 oder 2 Faktoren | > 3 Faktoren oder bekannte PAVK / KHK |
Troponin | Normal | 1-3x Normalwert | > 3x Normalwert |
STEMI / OMI - akuter Myokardinfarkt
ASS 250mg iv.
Heparin 5000IE iv. (bzw. 70 IE/kg)
Analgesie / Anxiolyse (z.B. Morphin, Benzodiazepin)
Betablocker z.B. Metoprolol 2mg iv. (wenn kein Schock, RRsyst >120mmHg, HF >50/min)
Checkliste STEMI / Hochrisiko-EKG ("OMI")
- Herzkatheter sofort (<2h)
- O2-Gabe bei SpO2 <90%, akuter Dyspnoe, Schock oder Periarrest
- ASS 150-300mg po. oder 250mg iv.
- Antikoagulation (auch bei bestehender OAK)
- Heparin: UFH 70 IE/kg iv. (pragmatisch: 5000 IE iv.)
oder Enoxaparin 0,5mg/kg iv. - (Bekannte HIT: Bivalirudin 0,75mg/kg iv. Bolus, dann 1,75mg/kg/h iv. für bis 4h nach Eingriff)
- Heparin: UFH 70 IE/kg iv. (pragmatisch: 5000 IE iv.)
- Anxiolyse (z.B. Midazolam 1-2mg iv. Boli) und/oder Analgesie (z.B. Morphin 2-3mg iv. Boli).
Ziel: Symptomlinderung, Verminderung myokardialer O2-Verbrauch - Betablocker (z.B. Metoprolol 2-5mg iv. Boli)
nicht bei RRsyst <120mmHg, HF<50/min., akute Herzinsuffizienz/kardiogener Schock - ev. Nitrate (Nitroglycerin 1-2 Hub sl.) zur Symptomlinderung
nicht bei Systolikum, Aortenklappenstenose, RRsyst <120mmHg, V.a. Rechtsherzinfarkt - P2Y12 Rezeptorantagonisten:
Unterschiedliche lokale Vorgaben, häufig periinterventionelle Gabe direkt im Katheterlabor
P2Y12 Rezeptorantagonisten - Initialbolus
- Prasugrel 60mg po., dann 10mg/24h po. (<60kg / >75J: 5mg)
- Ticagrelor 180mg po., dann 90mg/12h
- Clopidogrel 600mg po., dann 75mg/24h
- Cangrelor 30µg/kg iv., dann 4µg/kg/min iv.
Spezielle Situationen bei dringender Herzkatheteruntersuchung
- Bekannte Niereninsuffizienz
- Keine Kontraindikation in der Akutphase (ggf. Dialyse)
- Auf ausreichende Hydrierung achten
- Generell: Minimierung der Kontrastmittelgabe
- Nephrotoxische Medikamente möglich frühzeitig absetzen
- Antidiabetische Medikamente
- Metformin absetzen (im besten Fall 48h vor Intervention)
- Sulfonylharnstoffe pausieren bei nüchternen Patient:innen
- Hyperthyreose
- Perchlorat + Thiamazol
- Im Notfall (keine Vorwerte, bekannte Hyperthyreose): Natriumperchlorat 4ml (je nach Präparat ca. 60-84gtt), weitere Therapie nach Labor (nach/während Herzkatheter: TSH, fT3, fT4 bestimmen)
- Kontrastmittelallergie
- Evaluation: Besteht wirklich eine Kontrastmittelallergie? (Hautausschlag + Dyspnoe, Kreislaufdysregulation?) oder doch Kontrastmittelunverträglichkeit (Übelkeit, Erbrechen, passagere Sehstörungen)?
- Im Zweifel oder bei bestätigter Allergie: Prednisolon 100mg iv., Dimetinden 0,1mg/kg iv.) so früh wie möglich (<2h vor Exposition) - engmaschige klinische Überwachung, Adrenalin bereithalten (s. Anaphylaxie)
Lysetherapie bei OMI
Kaum noch Indikation bei ACS - nur bei STEMI/OMI und nicht-Verfügbarkeit Herzkatheter >120min (Diagnose bis Intervention) erwägen.
Bei Vorstellung >3h nach Beschwerdebeginn: Lyse kritisch hinterfragen, Effizienz deutlich abfallend. Spätestens nach Lyse sofortige Verlegung in PCI-Zentrum!
Vorgehen "OMI" + Lyse-Indikation
- ASS 250mg iv.
- Loading nach Rücksprache Zentrum (z.B. Clopidogrel 300mg po., (>75 Jahre: 75mg)
- Lyse möglichst binnen 10min (Lyse-Tabellen)
- Nach Lyse bis zur Revaskularisierung volle Antikoagulation z.B. mit
- Heparin 60-80IE/kg iv. Bolus, dann Heparin-Perfusor
- Nach Lyse bis zur Revaskularisierung volle Antikoagulation z.B. mit
- PCI nach Lyse binnen 2(-24)h
NSTEMI / NOMI
= kein STEMI und kein Hochrisiko-EKG jedoch erhöhtes Troponin. Abklärung nach Algorithmus inkl. Verlaufs-Troponin(e).
Checkliste NSTEMI ohne Hochrisko-EKG ("NOMI")
- Herzkatheter zeitnah (<24h)
- ggf. konservatives Management nach Maßgabe Kardiologie
- bei Risikokonstellation früher Herzkatheter
Risikokonstellation bei NSTEMI
Pat. mit ACS, kein STEMI, kein Hochrisiko-EKG, aber:
- Schock
- Akute Herzinsuffizienz
- Bedrohliche Arrhythmie(n)
- Persistierende Beschwerden
- EKG-Dynamik
- Neue Wandbewegungsstörung im Echo
- Massive Troponindynamik ("explodierendes Troponin") in Troponin-Kontrollen
→ Herzkatheter auch frühzeitiger erwägen, Rücksprache Kardiologie!
- O2-Gabe bei SpO2 <90%, akuter Dyspnoe oder Schock / Periarrest
- ASS 150-300mg po. oder 250mg iv.
- Antikoagulation (nicht bei bestehender OAK)
- UFH 70 IE/kg iv. (dann Heparin-Perfusor aPTT-Ziel 60-80) oder Enoxaparin 1mg/kg/12h sc.
- Falls konservatives Management: Fondaparinux 2,5mg sc./24h oder Enoxaparin sc. 1mg/kg/12h (GFR <30ml/min: 1mg/kg/24h)
- Anxiolyse, Betablocker analog zu STEMI
- P2Y12 Rezeptorantagonisten bei geplantem Herzkatheter meist periinterventionell, analog zu STEMI
Typ-2 Myokardinfarkt
Auch abseits der akuten Okklusion einer Koronarie kann es zu myokardialer Ischämie mit typischer ACS-Klinik (inkl. EKG-Veränderungen und Troponin-Anstieg) kommen - durch verminderte myokardiale Sauerstoff-Versorgung (meist in Kombination bestehender nicht-kritischer Koronarstenose).
Verdächtiges EKG bei meist kritisch krank wirkenden Pat.: Sog. "Hauptstamm-EKG".
→ Ziel: Stabilisierung + Therapie der Grunderkrankung, dann weitere kardiologische Evaluation, keine unreflektierte "ACS-Therapie" (z.B. wäre ASS/Heparin bei kritischer GI-Blutung potenziell fatal)
Typische Ursachen:
- Schock (z.B. bei Sepsis oder GI-Blutung)
- Tachykarde Rhythmusstörung (hämodynamisch wirksam)
- Anämie (oft akut auf chronisch)
- Vasospasmus (s. unten)
Vasospastische Angina
Spasmus von Koronargefäßen, a.e. im Rahmen von Hyperreagibilität der glatten Muskulatur. Risikofaktoren: Nikotinkonsum, Drogenkonsum. Typisch: Rasche Besserung nach Nitro-Gabe.
Ursachen:
- Vasospasmus bei Hyperreagibilität, ggf. verstärkt z.B. durch sympathomimetische Stimulation
- z.B. Kokain-Konsum / Intoxikation
- "Kounis-Syndrom": Vasospasmus durch Histaminfreisetzung im Rahmen von Anaphylaxie
Therapie:
- Analog zu ACS inkl. Herzkatheter (primär Evaluation: Andere Ursache für Typ 2 Myokardinfarkt?)
- Bei V.a. zusätzliche Anaphylaxie entsprechende Therapie (insb. Prednisolon 100mg und H1-Blocker (z.B. Dimetinden 0,1mg/kg iv.; Adrenalin im./iv. in diesem Fall eher zurückhaltend / Einzelfallentscheidung nach vorrangigem Problem)
Akutes Aortensyndrom
Einteilung (pragmatisch zudem "kompliziert / nicht kompliziert"):
- Aortendissektion (Notfallmedizisch höchste Relevanz)
- Stanford Typ A (Beteiligung Aorta Ascendens)
- Stanford Typ B (keine Beteiligung Aorta Ascendens)
- intramurales Aortenhämatom
- penetrierendes Aortenulkus (PAU)
Risikofaktoren für Aortensyndrom (insb. Aortendissektion)
- Arterielle Hypertonie
- Rauchen
- Männliches Geschlecht
- Z.n. Aorta-Eingriff / -OP, Koronarangiografie
- Positive Familienanamnese
- Drogenabusus: Insb. Kokain, Amphetamine
- Fluorchinolone
- Genetische Prädispositionen z.B. bikuspide Aortenklappe, Marfan Syndrom, Ehler-Danlos-Syndrom, Loeys-Dietz-Syndrom, polyzystische Nierenerkrankung, Turner-Syndrom (Monosomie X)
- Entzündliche Aortitis (autoimmunologisch (z.B. Vaskulitis), infektös (z.B. Aortenklappenendokarditis, Syphilis))
Folgen / Komplikationen bei akuten Aortensyndrom
- Aortenruptur mit hämorrhagischen Schock
- Organ- und Extremitäten-Malperfusionssyndrom
- Typ A: RCA-Abriss mit myokardialer Ischämie / Perikardtamponade
- Typ B: Nierenversagen, Mesenterialischämie, Spinale Ischämie, Beinischämie
- Schlaganfall bei Abriss der hirnversorgenden Gefäße
- Retrograde Typ-A-Dissektion bei initialer Typ-B-Dissektion
- Rasche Vergrößerung Aortendurchmesser → hochgradige Aortenklappeninsuffizienz
- Fistelungen (aortopulmonal, aortoösophagal, aortocaval)
- Nicht beherrschbarer Schmerz
Aortendissektion
Oft diffuses Beschwerdebild mit hoher Mortalität. Pragmatischer Merksatz für verdächtige Symptomatik: „Thoraxschmerz +1“ (thorakale Beschwerden mit zusätzlicher Symptomatik) z.B.:
- Neurologische Symptome (insb. Paresen), auch intermittierend
- Synkope, Krampfanfall / konvulsive Synkope
- Schmerz im Bauch, Rücken oder Beinen (auch intermittierend)
Anamnestische Hinweise:
- Plötzlicher Beginn
- „reißend“ oder „scharf“ beschriebener Schmerz, evtl. „wandernd"
- Ausstrahlung in Bein(e), Rücken, Bauch
- „schlimmster jemals verspürter Schmerz“
- Z.n. herzchirurgischen Eingriffen oder Aortendissektion
- Familiäre Häufung von Aortensyndromen
- Bekanntes Marfan-Syndrom (oder andere genetische Prädisposition)
- chron. Kokain-/Amphetaminkonsum
Klinischer Score: Aortic Dissection Detection Risk Score (ADD-RS)
Bis kein universelles Scoring-System, mehrere publizierte Konzepte. Keines davon bisher als Leitlinienempfehlung für die Nutzung in der Notaufnahme, aber als Anhaltspunkt / Unterstützung erwägbar. Nutzung von AAD-RS + D-Dimere wird in einer aktuellen US-Leitlinie empfohlen.
- AAD-RS (→Aortic Dissection Detection Risk Score) in Kombination mit D-Dimeren (ADD-RS + D-dimer)
- Empfehlung (ACEP, USA 2025): AAD-RS ≤ 1 Punkte (geringes Risiko)
- D-Dimere < 500 ng/ml FEU: Akute nichttraumatische Aortendissektion kann ohne CT / alternative erweiterte Bildgebung ausgeschlossen werden
- Falls im fokussierten Ultraschall (in)direkte Zeichen einer Dissektion: Überspringen der D-Dimer-Testung, direkt erweiterte Bildgebung (z.B. CT-A)
- Empfehlung (ACEP, USA 2025): AAD-RS ≤ 1 Punkte (geringes Risiko)
- AORTAs Score
- V.a. Aortensyndrom, dann:
- je 1 Punkt für
- bek. Aortenaneurysma
- Pulsdefizit
- Neurologisches Defizit
- Stärkster Schmerz
- Akuter Schmerz
- 2 Punkte bei Schock / Hypotension
- Vorgehen:
- 0-1 Punkte: Altersadaptierter D-Dimer (Jahre * 10ng/nl), falls erhöht: Bildgebung (z.B. CT)
- ≥ 2 Punkte: Direkt Bildgebung (z.B. CT)
EKG:
- Bei Verlegung der Koronargefäße können ev. STEMI-Äquivalente beobachtet werden
- Grob: 1/3 der EKGs unauffällig, 1/3 mit unspezifischen ST-/T-Veränderungen, 1/3 Ischämiezeichen (auch intermittierend!)
Checkliste Aortensyndrom
- Klinisch hochgradiger Verdacht: Evtl. Sono, dann sofort CT-Diagnostik
- Klinisch intermediärer Verdacht: Rasches Sono, Labordiagnostik inkl. Troponin + D-Dimere.
Falls Sono + Labor unauffällig + Symptome rückläufig oder anderweitig erklärt + klinische Einschätzung weiterhin „unwahrscheinlich“: Verzicht auf CT möglich.
- Therapie Aortensyndrom:
- Analgesie z.B. mit Morphin 2,5-5mg iv./Fentanyl 50-100µg iv.
- Blutdruck- und Herzfrequenzsenkung (bei Blutdruckdifferenz li/re.: höherer Wert zählt)
- Herzfrequenz-Ziel <60/min.: Metoprolol 3-5mg iv. Boli oder Esmolol-Perfusor (alternativ ggf. Landiolol)
- Blutdruck-Ziel <100-120mmHg systolisch: Urapidil 5-10mg iv. Boli, ggf. als Urapidil-Perfusor (Cave bei Nitro: Reflextachykardie!)
- Anxiolyse (falls nötig) z.B. mit Midazolam 1-2mg iv. Boli
- Art. Blutdruckmessung (am Ort der besten Perfusion / höchstem Blutdruck; häufig A. rad. rechts) - möglichst Leisten freihalten für Kanülierung im Zentrum
- Verlegung / Intervention ist wichtiger als art. Blutdruckmessung: Abwägen!
- Antagonisierung etwaiger Antikoagulation
- Sofortige Kontaktaufnahme mit Herz-/Gefäßchirurgie
- Typ A-Dissektion (Beteiligung des Aortenbogens): Herzchirurgische OP
- Typ B-Dissektion: Gefäßchirurgische Intervention, ggf. auch konservatives Procedere
Ösophagusruptur
Ursachen + Hintergrund
Starkes Erbrechen oder iatrogene Verletzung führt zur Ruptur aller Wandschichten des Ösophagus, meistens im distalen Drittel links dorsolateral (hier geringster muskulärer Widerstand).
Ursachen:
- Boerhaave Syndrom
spontane Ösophagusruptur als Folge einer Drucksteigerung im Ösophagus beim Erbrechen mit Austritt von Mageninhalt in Mediastinum und Pleurahöhle - Spontane Ruptur nach iatroger Manipulation
z.B. nach Anlage einer Magensonde, Durchführung einer Endoskopie wie Magenspiegelung oder TEE → meist fallen diese bereits periinterventionell auf, sodass noch keine Kontamination mit Nahrungsresten oder Mageninhalt erfolgt ist (bessere Prognose, minimalinvasives Prozedere häufiger möglich) - Selten sekundäre Formen
Malignome, durch Fremdkörper, traumatisch
Symptomatik:
- Die „lehrbuchtypische“ Präsentation mit dem „Mackler Trias“ des Boerhaave Syndrom ist selten:
- Allgemeine Symptome (je nach Lokalisation der Ruptur)
- Dyspnoe, Tachypnoe
- Nacken-, Thorax- oder epigastrische Schmerzen bis hin zum akuten Abdomen
- Dysphagie, Dystonie
- Fieber
Checkliste Ösophagusruptur
- Bei Verdacht: Thorax-CT mit oralem KM
- Therapie symptomatisch (Antiemetika, Analgesie)
- Antibiose, z.B. Piperacillin/Tazobactam 4,5g iv.
- Akutkomplikationen (z.B. Pneumothorax) behandeln
- Notfallendoskopie, ggf. offene OP
- CAVE: Keine NIV bei respiratorischer Verschlechterung, sondern RSI und invasive Beatmung
- Keine "blinde" Magensonden-Anlage!
Perikarditis / Myokarditis
Neu: Inflammatorisches myoperikardiales Syndrom (IMPS; inflammatory myopericardial syndrome) als Überbegriff in der Initialphase vor definitiver Diagnosestellung.
Definitionen (pragmatisch):
- Perikarditis = Entzündung des Perikards (meist ohne Troponinerhöhung)
- Myokarditis = Entzündung des Herzmuskels (Troponinerhöhung, spricht für myokardiale Beteiligung, oft LV-Einschränkung)
- Formale Diagnosestellung eigentlich erst durch Myokardbiopsie, bei normaler EF (und geringer TBC-Inzidenz) wird in Industrieländern darauf meist verzichtet
Perimyokarditis oder Myoperikarditis?
- Überwiegende Myokarditis mit perikardialer Beteiligung = Perimyokarditis
- Überwiegende Perikarditis mit myokardialer Beteiligung = Myoperikarditis
In der akutmedizinischen Praxis nicht zielführend zu unterscheiden, im Folgenden als „Inflammatorisches myoperikardiales Syndrom (IMPS)“ bezeichnet.
Ursachen
- Überwiegend idiopatisch (mutmaßlich viral bedingt)
- Seltene Ursachen:
Symptomatik:
Oft unspezifisch, insbesondere:
- Schwäche / Müdigkeit / Leistungseinschränkung
- akute oder kürzliche "Grippe-artige" Symptomatik oder Gastroenteritis
- ev. Fieber
- Brustschmerz
- Typisch: Lagerungsabhängig, pleuritisch, scharf,
- eher (sub-)akut
- ggf. auch "ACS-typisch"
- Veränderungen im EKG (oft dynamisch!)
- typisch: ST-Hebungen, Konkav, mehrere Ableitungen / keine Zuordnung zu Versorgungsgebiet
- ggf. auch ST-Senkungen, T-Negativierung, QRS-Verbreiterung
- Verminderung der QRS-Amplitude (insb. bei großem Perikarderguss) bis hin zu elektrischem Alternans (bei "swinging heart")
- Ein "normales" EKG schließt IMPS nicht aus!
Typische / spezifische Symptome:
Perikarditis | Myokarditis / Perimyokarditis |
|---|---|
|
|
Risikozeichen IMPS
(vereinfacht / angepasst nach ESC Leitlinien 2025)
- Akute Herzinsuffizienz, starke Dyspnoe
- Synkope
- Bedrohliche Rhythmusstörungen (z.B. ventrikuläre Tachykardie oder höhergradiger AV-Block)
- Akut reduzierte Pumpfunktion (LV-EF <40%)
- Leicht reduzierte Pumpfunktion (LV-EF 41-49%): Intermed. Risiko
- Großer Perikarderguss > 2 cm (oder Zeichen von Perikardtamponade)
- Perikarderguss 1-2 cm: Intermed. Risiko
- Fieber > 38,0 °C
- Subakuter Beginn (kein akuter Beginn, sondern schleichend über mehrere Tage/Wochen)
- Nicht-Ansprechen auf NSAR nach mehreren Tagen
- Troponinerhöhung (V.a. Perimyokarditis/Myokarditis)
Ggf. erhöhtes klinisches Risiko
- Bestehende Immunsuppression
- Z.n. Trauma
- bestehende Antikoagulation (Phenprocoumon, DOAKs)
Checkliste V.a. Inflammatorisches myoperikardiales Syndrom (IMPS)
- Breite Abklärung inkl. Anamnese, Labor (inkl. Troponin, BNP), EKG, Thoraxröntgen, Echokardiografie
- Therapie-Ziele: Analgesie, Entzündungshemmung, Rezidivvermeidung
- Schonung, keine körperlichen Anstrengungen (bis Symptomfreiheit/ Normalisierung der Laborwerte)
- Medikamente „First Line“ (Initialdosis für 1-2 Wochen, weitere Therapie nach Maßgabe Kardiologie)
- NSAR (z.B. Aspirin 750-1000mg/8h po. oder Ibuprofen 600-800mg/8h po.)
- ggf. um PPI ergänzen bei erhöhtem GI-Blutungsrisiko
- Bei Perikarditis zusätzlich: Colchizin (für 3-6 Monate)
- <70kg und/oder Nierenfunktionseinschränkung: 0,5mg /24h po.
- ≥70kg; 0,5mg /12 h po.
- ggf. um Betablocker ergänzen (bei Ruhe-HF >75/min; für mind. 6 Monate)
- bei Herzinsuffizienz-Zeichen zusätzlich medikamentöse Herzinsuffizienz-Therapie (auf Station)
- NSAR (z.B. Aspirin 750-1000mg/8h po. oder Ibuprofen 600-800mg/8h po.)
- IMPS mit Risikofaktor:
- Stationäre Aufnahme
- Bei Troponinerhöhung und/oder schwerer LV-Einschränkung, Synkope oder Rhythmusstörung: EKG-Monitoring (Gefahr der malignen Rhythmusstörung: Tachykardie / Bradykardie)
- Bildgebung (MRT) und/oder Myokardbiopsie (nach Risikoeinschätzung / Kardiologie)
- Perikarditis ohne Risikofaktoren: Ev. ambulant möglich; klinische und laborchemische Verlaufskontrolle spätestens nach 7 Tagen
Perikarderguss
Perikarderguss und -tamponade können als Komplikation verschiedener Erkrankungen auftreten (viele davon mit Leitsymptom „Thoraxschmerz“).
Je nach Ursache ist die Entwicklung oft langsam (z.B. bei malignem Erguss, rheumatoide Erkrankungen, ev. bei Urämie) oder schnell/akut (Trauma: Extern, z.B. penetrierende Thoraxverletzung oder iatrogen, z.B. nach Schrittmachersonden-Anlage oder Herzkatheter sowie Aortendissektion)
Ziel in der Notfallmedizin: Erkennen des Perikardergusses, bevor es zur hämodynamischen Kompromittierungen (= Perikardtamponade) kommt.
Symptomatik:
Ein Perikarderguss ist meist asymptomatisch, eine Perikardtamponade zeigt sich als obstruktiver Schock mit oft unspezifischen Symptome:
Checkliste Perikarderguss
- Anamnese: Traumatische vs. nicht-traumatische Ursache:
- Kürzlich „herznaher“ Eingriff (Herzkatheter, Schrittmacher) oder Thoraxverletzung?
- Z.n Myokardinfarkt?
- Bekanntes oder vermutetes Malignom, rheumatische Erkrankung, Niereninsuffizienz?
- Klinischer Hinweis auf akutes Aortensyndrom? (Falls ja → s. Aortensyndrom oben)
- EKG:
- ggf. zentrale Niedervoltage mit „elektrischem Alternans“ (Amplitudenwechsel z.B. der QRS-Komplexe unabhängig von der Atmung), oft in Kombination mit Sinustachykardie
- Ultraschall: Mittel der Wahl zur Diagnose und zur Differenzierung anderer Erkrankungen
- Perikarderguss vorhanden? Dissektionsmembran (xiphoidal / abdominell) darstellbar?
- Zeichen für hämodynamische Instabilität?
- Einwärtsbewegung des rechten Vorhofes / des rechten Ventrikels in der Diastole (= MK + TK sind offen)
- VCI moduliert oder weit?
- Bei Echokardiografie-Erfahrung: Atemabhängiger Alternans Einstromgeschwindigkeit über MK oder TK (PW Doppler über der MK, Schwankungen „Max“ von mehr als 25 % als Zeichen für Perikardtamponade, entspricht dem „Pulsus Paradoxus“ in der körperlichen Untersuchung)
- Markierung der optimalen Punktionsstelle für Punktion: Ort der größten Erguss-Ausdehnung und kürzester Weg möglichst ohne „Hindernisse“ (Lunge, Leber) - s. Perikardpunktion
- Therapie:
- Perikardtamponade: Mittel der Wahl = Perikardpunktion (in der Notaufnahme immer ultraschallgezielt). Je nach lokalen Vorgaben ggf. Punktion im Herzkatheterlabor (mittels Durchleuchtung etc.), Vorgehen nach Klinik der Patient:in (Transport zumutbar?)
- Ausnahme: Penetrierendes Thoraxtrauma + Tamponade: Notfall-Thorakotomie
Tako Tsubo Kardiomyopathie
z.B. auch „Stress-Kardiomyopathie“, „Stressinduzierte Kardiomyopathie“ oder „Broken-Heart-Syndrom“).
Kardiomyopathie mit meist deutlicher Einschränkung der LV-Pumpfunktion, typische apikale Hypo-/Akinesie mit „apical ballooning“. Primär symptomatische Therapie - meist gute Erholung nach einigen Wochen.
Typische Symptomatik:
- Thoraxschmerz
- ST-Hebungen / T-Negativierungen
- Troponin-Erhöhung
- Atemnot
- evtl. Rhythmusstörung (bis hin zu VT / Kammerflimmern)
- evtl. Synkope
Hintergrund und Diagnostik
Akute, stressinduzierte, reversible Dysfunktion des linken Ventrikels. Typischerweise in Europa betroffen: Frauen mittleren Alters (aber: Jedes Geschlecht und Altersgruppe möglich)
Auslöser meist emotionaler Stress (selten auch „positive“ Situationen), auch akute Erkrankungen (insb. Neurologische Ereignisse) / OPs mit darauf folgenden „Katecholaminsturm“ (massiv erhöhte endogene Katecholamine).
Seltene (atypische) Varianten:
- Mittelventrikulärer Typ (v.a. Hypokinesie des mittleren Ventrikels)
- basaler Typ (basale Hypokinesie)
- fokaler Typ (isoliertes Segment mit Hypokinesie, insb. Anterolateral)
- global (globale Hypokinesie); selten
Diagnostik:
- Ausschlussdiagnose! Beinahe immer Herzkatheter zum Ausschluss eines ACS notwendig
- Andere DD erwägen (inkl. Aortensyndrom)
- Typische Befunde
- EKG
- Meist ausgeprägtes „STEMI/OMI EKG“
- Oft ausgedehnte T-Negativierungen (ggf. über Koronar-Versorgungsgebiet hinausgehend
- Evtl. QTc Verlängerung mit Risiko für Torsade de Pointes Tachykardie
- Labor
- Troponin oft eher gering erhöht (relativ zu oft ausgeprägten ST-Veränderungen und Pumpfunktionseinschränkung
- Häufig relevante BNP/NtProBNP - Erhöhung
- Echokardiografie
- Vorwiegend apikale Akinesie, hierdurch bedingte Ballonierung der Herzspitzenregion (außer bei atypischen Varianten, siehe oben)
- Reduzierte linksventrikuläre Pumpfunktion
- Auf apikalen Thrombus, Obstruktion des LV-Ausflusstraktes, Mitralinsuffizienz achten
- Herzkatheter mit Ausschluss KHK
- Im stationären Verlauf typischerweise Kardio-MRT nötig zum Ausschluss Myokarditis oder MINOCA (Myokardinfarkt ohne obstruktive Koronarsklerose)
- EKG
Checkliste V.a. Tako-Tsubo-Kardiomyopathie
- Ausschluss anderer akuter Ursachen
- Herzkatheter (STEMI/OMI - koronare Ursachen für EKG-Veränderung / Pumpschwäche ausschließen
- Erwägen: Phäochromozytom, andere Ursache für Katecholaminsturm z.B. Hirnblutung
- Kreislaufunterstützung
- Vorsicht mit Katecholaminen (evtl. Verschlechterung der Symptomatik)
- Im Notfall ggf. linksventrikuläres Unterstützungssystem (ECMO, Impella® etc.)
- Allgemeine Therapie
- Antikoagulation (Risiko apikaler Thrombusbildung)
- Behandlung etwaiger Herzrhythmusstörungen
- Medikamentöse Herzinsuffizienztherapie (Betablocker, ACE-Hemmer, ggf. Diuretika etc.)
- Stationäre Überwachung (je nach Klinik zumindest Monitoring; häufig IMC / Intensiv)
Thoraxschmerz und Schwangerschaft
Schwangerschaft = "Stresstest"
Eine Schwangerschaft ist auch automatisch ein "Stresstest" für den Kreislauf:
- Erhöhter Sauerstoffbedarf durch den Fötus
- Kompensation: erhöhtes Atemminutenvolumen, erhöhtes Blutvolumen + Herzzeitvolumen.
- Folgen: Zunahme der links- und rechtsventrikulären Myokardmasse, Diastolische Dysfunktion (bei 20% der Schwangeren)
- Größenzunahme des Uterus
- VCI wird komprimiert (erniedrigter venöser Rückfluss)
- Aorta wird komprimiert (erhöhte Nachlast)
- Konsequenz: in Rückenlage daher insb. im dritten Trimenon Reduktion des HZV um 25% möglich, Beinödeme, Stase, Hyperkoagulabilität
Ziel in der Notaufnahme bei Thoraxschmerz von Schwangeren ist Differenzierung zwischen „normale“ Veränderungen in der Schwangerschaft, die zu Beschwerden führen können und gefährlichen Ursachen.
Schwangerschaftsbeschwerden und gefährliche Ursachen von Thoraxschmerz
„Normale" Schwangerschaftsbeschwerden (siehe Schwangerschaft)
- Reflux
- Rippenschmerzen
- Erhöhtes Atemminutenvolumen
- Erhöhte Herzfrequenz
Gefährliche Ursachen bei Thoraxschmerz in der Schwangerschaft
- Schwangerschaftskardiomyopathie
- Nicht-ischämisch dilatativ, EF< 45%, keine andere Ursache eruierbar
- bis 5 Monate postpartal möglich
- Risikofaktoren: Schwangerschaftshypertonie, Zwillinge, ↑Alter Mutter
- EKG, Echokardiografie (BNP meistens nicht hilfreich, da generell erhöht in der Schwangerschaft)
- Symptomatische Therapie
- s. Herzinsuffizienz
- Myokardinfarkt / SCAD (spontane Koronardissektion)
- Lungenembolie
- YEARS-Kriterien (s. oben) für Schwangere evaluiert und anwendbar
- Eine übersehene Lungenarterienembolie ist gefährlicher für Mutter und Kind als ein CT!
- Lyse ist nicht kontraindiziert in der Schwangerschaft
- Aortendissektion (s. oben)
Risikofaktoren für gefährliche Ursachen von Thoraxschmerzen in der Schwangerschaft:
- Herkunft (Frauen mit afrikanischer Herkunft haben ein 3-4x erhöhtes Risiko für gefährliche Ursachen)
- Alter >40 Jahre
- Hypertonie in der Schwangerschaft (deutlich erhöhtes Risiko für Myokardinfarkt und Herzinsuffizienz)
- Übergewicht (assoziiert mit Schlafapnoe)
Nicht kardiopulmonale Ursachen
Thoraxschmerz kann durch eine Vielzahl an Erkrankungen verursacht sein. Die meisten gefährlichen bzw. akut lebensbedrohlichen Ursachen sind kardiopulmonal / vaskulär (ACS, Aortendissektion, Pneumothorax, Lungenembolie), zusätzlich muss auch die Ösophagusruptur initial erwogen werden.
Falls diese bedrohlichen Ursachen ausgeschlossen bzw. differentialdiagnostisch verworfen sind, können weitere Erkrankungen erwogen werden (hier pragmatische Übersicht).
Wichtig: Wenn die Diagnose nicht völlig klar ist, sollte auch bei Entlassung auf das „Erfinden“ von Diagnosen oder Ursachen unbedingt verzichtet werden.
"Red Flag": Wiedervorstellung / erneute Alarmierung Rettungsdienst. Dann "ungefährliche Vordiagnose" doppelt kritisch hinterfragen!
Gastrointestinale Erkrankungen
Potentiell häufige Ursache, Symptome können vom Schmerzcharakter und Lokalisation sehr ACS-typischen Symptomen ähneln.
Gastrointestinale - thorakale Beschwerden
Beginn / Dauer | Qualität / Lokalisation | Kommentar | |
|---|---|---|---|
Gastroösophagealer Reflux | Zeitnah nach dem Essen | "Brennen" substernal / epigastrisch | verstärkt bei postprandialem Hinlegen, Besserung nach Antazida/PPI |
Dyspepsie / Gastritis | unspezifisch, teils postprandial verstärkt | Druckgefühl, ev. mit Übelkeit, Aufstoßen, „gebläht“ | Oft bereits bekannte, rezidivierende Beschwerden |
Peptisches Ulkus (Magen-/Duodenum) | 1-3 Stunden nach dem Essen auftretend | Brennen epigastrisch | typisch Duodenum: Initial Besserung durch Nahrungsaufnahme Magenulkus: ev. auch Verschlechterung durch Nahrung |
Ösophagusspasmen | unspezifisch | sehr starke Schmerzen Druck, Enge, Brennen retrosternal oft „wellenförmig“ | CAVE: ev. Besserung auf Nitro und Calciumantagonisten! |
Hepatobiliäre Erkrankung, z.B. Cholezystitis, Pankreatitis | Häufig postprandial verstärkt | Schmerzen ev. kolikartig, Druckgefühl Epigastrisch, rechter Oberbauch |
Bewegungsapparat / Neuromuskulär
In der Notaufnahme ist eine Festlegung einer speziellen muskulären / muskuloskelettalen Erkrankung oft erschwert. Teils lässt sich eine Anamnese mit zeitlichem Zusammenhang der Beschwerden nach vermehrter körperlicher / sportlicher Aktivität erheben (hier muss oft explizit nachgefragt werden).
Auch rheumatische und verwandte Erkrankungen können Thoraxschmerzen verursachen, haben jedoch meist zusätzliche Symptome (z.B. Rheumatoide Arthritis, Fibromyalgie, Osteoporose mit spontaner Fraktur).
Checkliste unkomplizierte muskuloskelettale thorakale Beschwerden
- Schonung
- Analgesie, z.B. mit NSAR (Ibuprofen) oder Paracetamol
- Ambulante Verlaufskontrolle
- Wiedervorstellung bei Verschlechterung oder Risikozeichen (vegetative Symptomatik, (Prä)Synkope, Atemnot etc.
Muskuloskelettale thorakale Beschwerden
Beginn / Dauer | Qualität / Lokalisation | Kommentar | |
|---|---|---|---|
Costochrondritis / "Tietze Syndrom" | variabel | Schmerzen, durch lokalen Druck auslösbar | Costochrondrale Gelenke gereizt =, durch Druck auslösbar |
Zervikale Bandscheiben-erkrankung | variabel / plötzlich | Schmerzen, ev. Taubheitsgefühl im Arm Begrenzt lokalisiert mit Ausstrahlung in die Arme/Schulter | Verstärkung ggf. bei Halsbewegungen/ Rotation BWS |
Überlastung (Trauma) der WS | meist konstant, chronisch | Schmerzen begrenzt lokalisiert auf den entsprechenden Bereich der WS | Verstärkung durch Bewegung / Rotation |
Osteoporose bzw. Metastasen: Spontane Rippen- / Wirbelsäulenfraktur | meist akut | Starke lokalisierte Schmerzen | bek. Osteoporose, anmnestisch / klinischer Verdacht DD Malignom: Großzügig Röntgendiagnostik |
Herpes Zoster
In der Initialphase kann Herpes Zoster auch thorakale Beschwerden verursachen. Typisch ist der scharf-brennend, dermatombezogener Schmerz, oft zeigen sich bei genauerer Untersuchung schon erste Hauterscheinungen.
Therapie und Details s. Herpes Zoster
Psychische Auslöser
Bis zu 10% der Patient:innen, die mit akuten Thoraxschmerzen in die Notaufnahme kommen, haben eine Panikstörung oder eine ähnliche Erkrankung. Situative Faktoren können bei zugrunde liegender Panikstörung oder Depression häufig thorkales Unwohlsein (oft als Engegefühl beschrieben, selten als klassischer Schmerz) und Dyspnoe auslösen. Die Lokalisation kann variabel sein.
Bei Patient:innen mit KHK und Z.n. Myokardinfarkt werden auch (ähnlich einer PTBS) stress- / oder belastungsbedingt thorakales Unwohlsein beschrieben. Aufgrund des hohen Risikos der Vorerkrankung muss jedoch bei bekannter KHK jedenfalls eine gründliche Abklärung wie bei Akutem Koronarsyndrom erfolgen.
Wichtig: Diagnose nicht primär in der Notaufnahme stellen - Ausschlussdiagnose!
Weiterführende Literatur und Links
Interessante Links (frei zugänglich)
- ESC Leitlinie Perikarditis und Myokarditis (ESC 2025)
- ECG Patterns of Occlusion Myocardial Infarction (2025, open access)
- ESC Leitlinie ACS (ESC 2023)
- HEART Score Informationen (Heart Score)
- AHA Leitlinie Aortenerkrankungen (AHA 2022)
- Hochrisiko-EKGs inkl. Infografik (Nerdfallmedizin 2021)
- AHA Leitlinie Brustschmerz (AHA 2021)
- Empfehlungen ACS + NOAKs (DGK 2021)
- ESC Leitlinie ACS ohne ST-Hebungen (ESC 2020)
- ESC Leitlinie ACS mit ST-Hebungen (ESC 2017)
- ESC Leitlinie Perikard-Erkrankungen (ESC 2015)
Literatur
- Schulz-Menger, J. u. a. 2025 ESC Guidelines for the management of myocarditis and pericarditis. Eur. Hear. J. ehaf192 (2025)
- Promes, S. B., Westafer, L., Byyny, R. & Diercks, D. B. Critical Issues in the Evaluation and Management of Adult Patients With Suspected Acute Nontraumatic Thoracic Aortic Dissection. Ann. Emerg. Med. 86, e12–e26 (2025).
- Ricci, F. et al. ECG Patterns of Occlusion Myocardial Infarction: A Narrative Review. Ann. Emerg. Med. (2025)
- Morello, F. u. a. Diagnosis of acute aortic syndromes with ultrasound and d-dimer: the PROFUNDUS study. Eur. J. Intern. Med. 128, 94–103 (2024).
- Byrne, R. A. et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur. Hear. J. (2023).
- McLatchie, R. et al. Diagnosis of Acute Aortic Syndrome in the Emergency Department (DAShED) study: an observational cohort study of people attending the emergency department with symptoms consistent with acute aortic syndrome. Emerg. Med. J. 1–9 (2023).
- Knapsis, A. & Süss, J. D. Das akute Aortensyndrom. Notaufnahme up2date 05, 41–58 (2023).
- Isselbacher, E. M. et al. 2022 ACC/AHA Guideline for the Diagnosis and Management of Aortic Disease. Circulation 146, e334–e482 (2022).
- Singh, T. u. a. Takotsubo Syndrome: Pathophysiology, Emerging Concepts, and Clinical Implications. Circulation 145, 1002–1019 (2022).
- Gulati, M. et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR Guideline for the Evaluation and Diagnosis of Chest Pain: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation 144, e368–e454 (2021).
- Hamm, C. W. et al. Empfehlungen zur prähospitalen Behandlung des akuten Koronarsyndroms bei Patienten unter Dauertherapie mit neuen oralen Antikoagulanzien (NOAKs). Kardiologe 15, 32–37 (2021).
- DGG. S2k-Leitlinie Typ B Aortendissektion. AWMF (2021).
- Fessele, K., Fandler, M. & Gotthardt, P. Hochrisiko-EKG bei akutem Thoraxschmerz. Med. Klin. - Intensiv. Notfallmedizin 117, 510–516 (2021).
- Grautoff, S., Fessele, K., Fandler, M., Knappen, N. & Gotthardt, P. „STEMI mimics“. Med. Klin. - Intensiv. Notfallmedizin 118, 35–44 (2021).
- Collet, J.-P. et al. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur. Hear. J. 42, ehaa575 (2020).
- Behm, P. & Westenfeld, R. Leitsymptom Thoraxschmerz – akutes Koronarsyndrom. Notaufnahme up2date 2, 123–138 (2020).
- Morello, F. et al. Development and Validation of a Simplified Probability Assessment Score Integrated With Age‐Adjusted d‐Dimer for Diagnosis of Acute Aortic Syndromes. J. Am. Hear. Assoc. 10, e018425 (2020).
- Weinreich, M. et al. Computer-aided detection and identification of implanted cardiac devices on chest radiography utilizing deep convolutional neural networks, a form of machine learning. J. Am. Coll. Cardiol. 73, 307 (2019).
- Brady, W. & Souza, K. de. The HEART score: A guide to its application in the emergency department. Turk. J. Emerg. Med. 18, 47–51 (2018).
- Ibanez, B. et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur. Hear. J. 39, 119–177 (2017).
- Body, R. et al. Troponin-only Manchester Acute Coronary Syndromes (T-MACS) decision aid: single biomarker re-derivation and external validation in three cohorts. Emerg. Med. J. 34, 349 (2017).
- Kounis, N. G. Kounis syndrome: an update on epidemiology, pathogenesis, diagnosis and therapeutic management. Clin. Chem. Lab. Med. (CCLM) 54, 1545–1559 (2016).
- Adler, Y. et al. 2015 ESC Guidelines for the diagnosis and management of pericardial diseasesThe Task Force for the Diagnosis and Management of Pericardial Diseases of the European Society of Cardiology (ESC) Endorsed by: The European Association for Cardio-Thoracic Surgery (EACTS). Eur. Hear. J. 36, 2921–2964 (2015).
- Templin, C. u. a. Clinical Features and Outcomes of Takotsubo (Stress) Cardiomyopathy. N. Engl. J. Med. 373, 929–938 (2015).
- Erbel, R. et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases. Eur. Hear. J. 35, 2873–2926 (2014).
- Backus, B. E. et al. A prospective validation of the HEART score for chest pain patients at the emergency department. Int. J. Cardiol. 168, 2153–2158 (2013).